Per
fissato numero atomico (Z), al progressivo allontanarsi dagli isotopi stabili (verso sinistra, cioè per masse atomiche minori, oppure verso destra, cioè per masse atomiche maggiori), i tempi di decadimento dei vari
isotopi diminuiscono sempre più, sino a raggiungere valori infinitesimi. E’ quindi intuitivo immaginarsi la valle di stabilità ß come una valle molto stretta, con gli isotopi stabili distribuiti sul fondovalle e gli
isotopi instabili lungo le pareti, a diverse altezze in base al loro tempo di decadimento (sempre più rapidi a mano a mano che ci si allontana dal fondo). Di qui il nome di valle di stabilità ß.
Il processo s, costituito
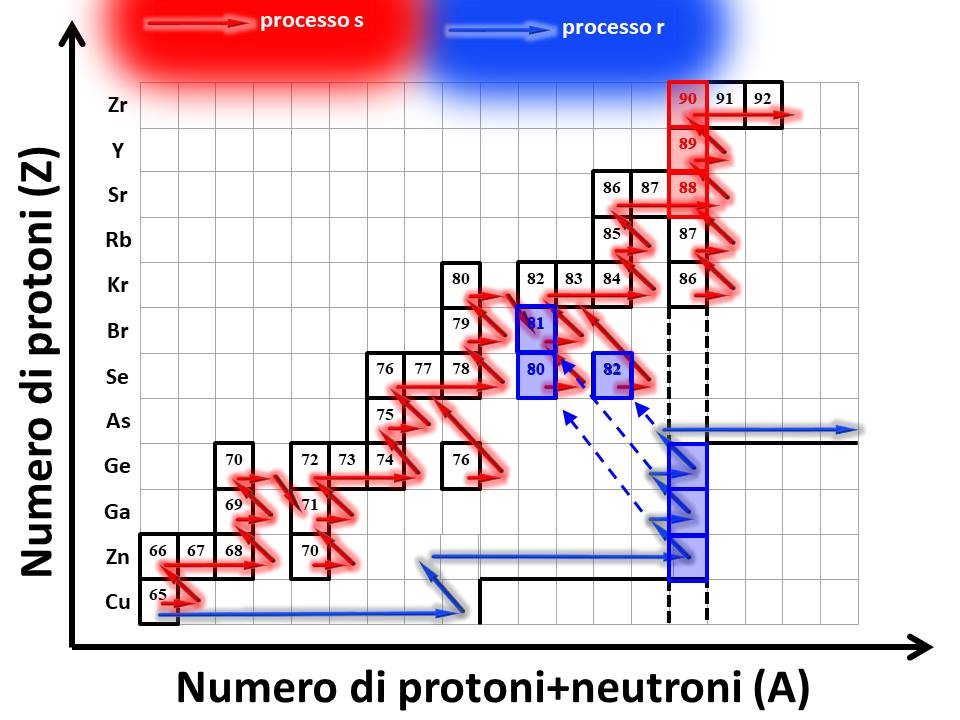
dalla sequenza di freccette orizzontali rosse (ognuna di esse rappresenta una cattura neutronica), avviene SEMPRE in prossimità della valle di stabilità ß. Quando un nucleo stabile cattura un neutrone creando un isotopo
instabile, quest’ultimo ha il tempo di decadere nel suo isobaro stabile (ossia un nucleo stabile avente la stessa massa atomica, ma un diverso numero di protoni) prima di catturare un altro neutrone. Questi decadimenti possono essere di tipo ß+
(un protone
si trasforma in un neutrone: frecce rosse verso il basso) oppure ß- (un neutrone
si trasforma in un protone: frecce rosse verso l’alto).
Lungo il percorso del processo s, esistono nuclei le cui configurazioni nucleari
particolarmente stabili (sono detti nuclei “magici”) fanno si che i rispettivi elementi si accumulino rispetto a quelli vicini (caselle rosse colorate). Di conseguenza, vengono a crearsi veri e propri
“picchi” nella
distribuzione degli elementi pesanti creati attraverso il processo s (in corrispondenza di numeri di neutroni N=50, N=82 ed N=126).
Questo è illustrato in Figura 3, che mostra come
il processo s presenti 3 picchi ben
distinti: il primo in corrispondenza del gruppo stronzio-ittrio-zirconio (Sr-Y-Zr), il secondo del gruppo bario-lantanio-cerio-neodimio (Ba-La-Ce-Nd) ed il terzo
in corrispondenza del piombo (Pb). Il processo s
produce circa la metà degli elementi più pesanti del ferro presenti nell’Universo.
La restante metà è creata attraversa il processo di cattura neutronica rapido (processo r).In questo caso, attraverso
una serie di catture neutroniche successive su un singolo isotopo stabile si possono produrre isotopi molto lontani dalla valle di stabilità ß (frecce orizzontali blu in Figura 9). Infatti, a causa dell’elevatissimo flusso di neutroni, infatti, i nuclei
instabili appena sintetizzati non hanno il tempo di decadere e sono costretti a loro volta a catturare un neutrone. Questa successione di catture neutroniche procede sino a creare nuclei con tempi di vita infinitesimi
(millesimi di secondo). A questo punto il decadimento ß è più veloce della cattura neutronica e
il nucleo può decadere, aumentando la propria carica (frecce blu verso l’alto). In corrispondenza
dei nuclei magici di neutroni (vedi sopra) abbiamo nuovamente
l’accumulo di alcuni elementi (caselle blu colorate). Una volta terminato il flusso di neutroni, questi isotopi possono poi decadere nei relativi isobari stabili lungo la valle di stabilità . In
Figura 3, di conseguenza, appaiono altri tre picchi, caratteristici del processo r: il primo in corrispondenza di selenio-bromo-kripton (Se-Br-Kr), il secondo di
tellurio-iodio-xenon (Te-I-Xe) ed il terzo di iridio-platino-oro (Ir-Pt-Au). Infine, facciamo notare che anche gli elementi radioattivi
terrestri con vita media molto lunga (come il torio e l'uranio) sono stati creati
attraverso il processo r.
Abbiamo visto come i due processi di cattura neutronica appena descritti siano estremamente diversi. E’ strabiliante come tutti gli elementi chimici pesanti siano stati creati in condizioni
così differenti e uniche (vi sono altri processi
intermedi, la cui rilevanza è però decisamente trascurabile rispetto alle due componenti principali s ed r). Resta ancora un argomento da sviscerare: DOVE avvengono questi processi? Questa domanda ha tenuto
occupati gli astrofisici nucleari negli ultimi 40 anni...e ancora fa passare loro notti insonni!!!
Due sono gli ambienti stellari di nostro interesse: le stelle di piccola massa durante la loro fase evolutiva di Ramo
Asintotico (per il processo s) ed i sistemi binari composti da due stelle di neutroni
(per il processo r).